제넥신은 인도네시아 식약처(BPOM)에서 코로나19 백신 후보물질(GX-19N)의 임상 2·3상 시험계획을 승인받았다고 7월 7일 밝혔다. 한국내에서 개발 중인 백신 후보물질이 글로벌 임상 2·3상 승인을 받은 최초 사례다.
제넥신은 인도네시아의 세계 4위 인구 규모와 최근 변이에 따른 코로나19 확산세에 따라 임상 대상자 모집과 연구가 수월할 것으로 보고 있다.
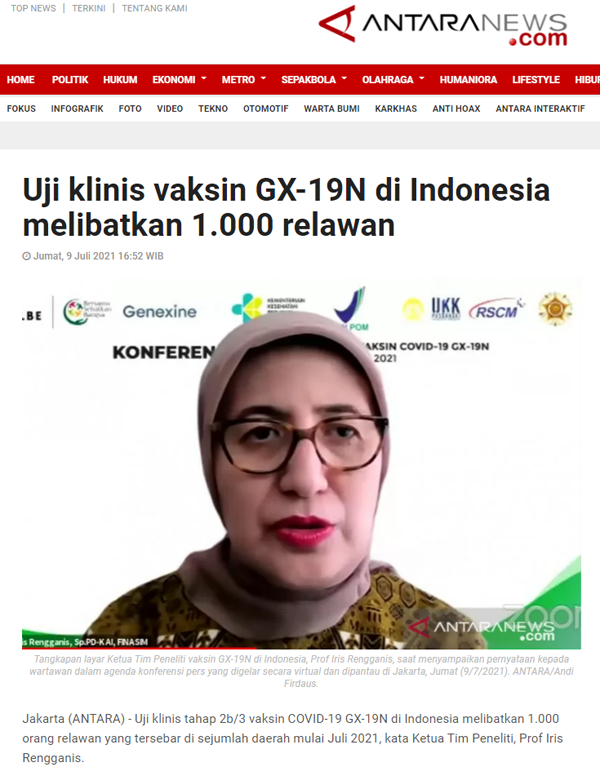
GX-19N은 제넥신 컨소시엄(제넥신, 제넨바이오, 바이넥스, SL백시젠, 포스텍, 국제백신연구소, 카이스트)이 개발 중인 DNA 기반의 코로나19 백신 후보물질이다. 인도네시아 의과대학 아이리스 렝가니스 GX-19N 백신 임상 연구단장의 인터뷰 내용을 아래와 같이 요약한다.
“2021년 7월부터 코로나19 GX-19N 백신의 2상/3상 임상 시험이 인도네시아 여러 지역에서 1,000명의 지원자가 참여한다. 우리는 FKUI 연구 센터와 RSCM을 의뢰 병원으로 모집했으며 자카르타, 데폭, 버카시, 욕야카르타, 솔로 및 클라텐에서 참여한다.
PT Kalbe Farma Tbk가 COVID-19 GX-19N 백신에 대한 2상/3상 임상 시험을 수행하기 위해 식품 의약 감독청 (BPOM)의 승인을 받았다. 임상 시험은 2021년 7월에 시작되며 2021년 말까지 안전성 및 효능에 대한 중간 분석을 수행 할 예정이다.
 GX-19N 코로나19 백신이 다른 코로나19 백신과 다르다. 더 많은 바이러스 단백질을 암호화하는 DNA 기반 GX-19N COVID-19 백신은 더 높은 항체를 생성하고 체내에서 더 오래 지속될 것으로 보인다. GX-19N DNA 백신은 COVID-19 바이러스의 다양한 변종에 대한 보호 기능을 갖고 있는 탁월한 잠재력을 가지고 있는 것으로 보인다.
GX-19N 코로나19 백신이 다른 코로나19 백신과 다르다. 더 많은 바이러스 단백질을 암호화하는 DNA 기반 GX-19N COVID-19 백신은 더 높은 항체를 생성하고 체내에서 더 오래 지속될 것으로 보인다. GX-19N DNA 백신은 COVID-19 바이러스의 다양한 변종에 대한 보호 기능을 갖고 있는 탁월한 잠재력을 가지고 있는 것으로 보인다.
GX-19N 백신은 면역 증강제 바이러스 벡터와 보조제를 사용하지 않기 때문에 면역 체계가 약한 사람들에게 투여 될 가능성이 있다. 이 백신은 근육 세포에 직접 시키는 특수 장치를 사용하여 근육에 투여된다.
COVID-19 GX-19N 백신의 2상 /3상 임상 시험은 인도네시아 대학의 의학부, Cipto Mangunkusumo 및 Krida Wacana 대학 의학부, Gadjah Mada 대학 공중 보건 및 간호 대학 등 산학협력으로 이루어진다.
코로나19 GX-19N 백신이 정부 예방접종을 위한 것인지 아니면 상호 협력을 위한 것인지는 식약청(BPOM)으로부터 긴급사용승인(EUA-emergency use authorization) 허가를 받아야만 결정된다.” <안타라 통신 종합>





![[스타일코리안 인도네시아] MOIDA Gandaria City점 오픈](https://haninpost.com/wp-content/uploads/2026/05/스타일코리안인도네시아-MOIDA-Gandaria-City점-오픈-180x135.jpeg)







![[KOTRA] 인도네시아 무선이어폰 시장 트렌드, ‘가성비 경쟁’ 속 수요 지속 확대](https://haninpost.com/wp-content/uploads/2021/11/KOTRA-180x124.jpg)


![[그래픽] 트럼프·시진핑 베이징 정상회담, 협력확대 한목소리 냈으나 ‘대타협’ 없어](https://haninpost.com/wp-content/uploads/2026/05/트럼프·시진핑-2026-베이징-미중-정상회담-180x135.jpg)















![[KOTRA] 인도네시아 무선이어폰 시장 트렌드, ‘가성비 경쟁’ 속 수요 지속 확대](https://haninpost.com/wp-content/uploads/2021/11/KOTRA-238x124.jpg)



















 카톡아이디 haninpost
카톡아이디 haninpost

